Als Dave Dubin im Alter von 29 Jahren erfuhr, dass er Darmkrebs hatte, war das keine große Überraschung. Sein Großvater und sein Vater hatten beide die Krankheit überlebt. „Es war fast wie bei den Dubins, und wir haben einfach weitergemacht“, sagt Dubin. Er wurde operiert und erhielt eine Chemotherapie, aber 10 Jahre später kehrte der Krebs zurück. Genetische Tests fanden schließlich eine Erklärung für die Versuche seiner Familie: eine Mutation in einem DNA-Reparaturgen, das genetische Fehler in sich teilenden Zellen anhäufen lässt. Die Krankheit, das Lynch-Syndrom, ist mit einem lebenslangen Krebsrisiko von bis zu 70 % verbunden.
Dubin, 55, unterzieht sich jährlichen Darmspiegelungen, Endoskopien und bildgebenden Scans, bei denen ein dritter Krebs in seiner Niere entdeckt wurde. Sein ältester Sohn, Zach Dubin, 26, hat die DNA-Reparaturmutation geerbt und wird ebenfalls regelmäßig auf Krebs untersucht. „Es ist kein Spaß. Niemand hat Spaß daran“, sagt Dave Dubin – weder an der zweitägigen Vorbereitung auf die Darmspiegelung noch an der Sorge um mögliche Tumore. Die Krankheit hat ihn auch zu einem Aktivisten gemacht. Er und seine Familie in Haworth, New Jersey, gründeten die gemeinnützige Organisation AliveAndKickn, um die Forschung und das Bewusstsein für das Lynch-Syndrom zu fördern, von dem schätzungsweise 1,1 Millionen Menschen in den Vereinigten Staaten betroffen sind.
„In dieser Patientenpopulation gibt es viele Ängste“, sagt der Onkologe und Genetiker Eduardo Vilar-Sanchez vom MD Anderson Cancer Center. „Das ist eine große psychologische Belastung.“ In der Hoffnung, diese Belastung zu lindern, wird Vilar-Sanchez demnächst eine klinische Studie mit einem Impfstoff leiten, der Lynch-bedingte Krebserkrankungen verhindern oder zumindest verzögern soll. Wenn es klappt, sagt Dave Dubin, „könnte das ein Riesenerfolg sein“.
Impfstoffe zur Vorbeugung bestimmter Krebsarten gibt es bereits. Sie richten sich gegen Viren: das Hepatitis-B-Virus, das Leberkrebs auslösen kann, und das humane Papillomavirus, das Gebärmutterhalskrebs und einige andere Krebsarten verursacht. Die meisten Krebsarten werden jedoch nicht durch Viren verursacht. Die Lynch-Impfstoffstudie wird eine der ersten klinischen Tests eines Impfstoffs zur Verhinderung nichtviraler Krebsarten sein.
Die Idee besteht darin, Teile von Proteinen oder Antigenen aus Krebszellen in den Körper einzubringen, um das Immunsystem dazu anzuregen, beginnende Tumore anzugreifen. Das Konzept ist nicht neu, und es ist auf Skepsis gestoßen. Vor einem Jahrzehnt wurde in einem Nature-Leitartikel das Ziel einer prominenten Gruppe von Brustkrebsbefürwortern, bis 2020 einen präventiven Impfstoff zu entwickeln, als „fehlgeleitet“ abgetan, unter anderem wegen der genetischen Komplexität von Tumoren. Der Leitartikel bezeichnete das Ziel als „ein Ziel, das die Wissenschaft noch nicht erreichen kann“. Doch nun sind einige Teams – darunter eines, das von derselben Interessengruppe, der National Breast Cancer Coalition (NBCC), finanziert wird – bereit, präventive Impfstoffe zu testen, in einigen Fällen an gesunden Menschen mit hohem genetischem Risiko für Brust- und andere Krebsarten. Ihre Bemühungen wurden durch neue Erkenntnisse über die genetischen Veränderungen bei Krebs im Frühstadium sowie durch die Erkenntnis vorangetrieben, dass die Impfstoffe am besten bei gesunden Menschen wirken sollten, die noch nie an Krebs erkrankt waren, da selbst entstehende Tumore das Immunsystem unterdrücken können.
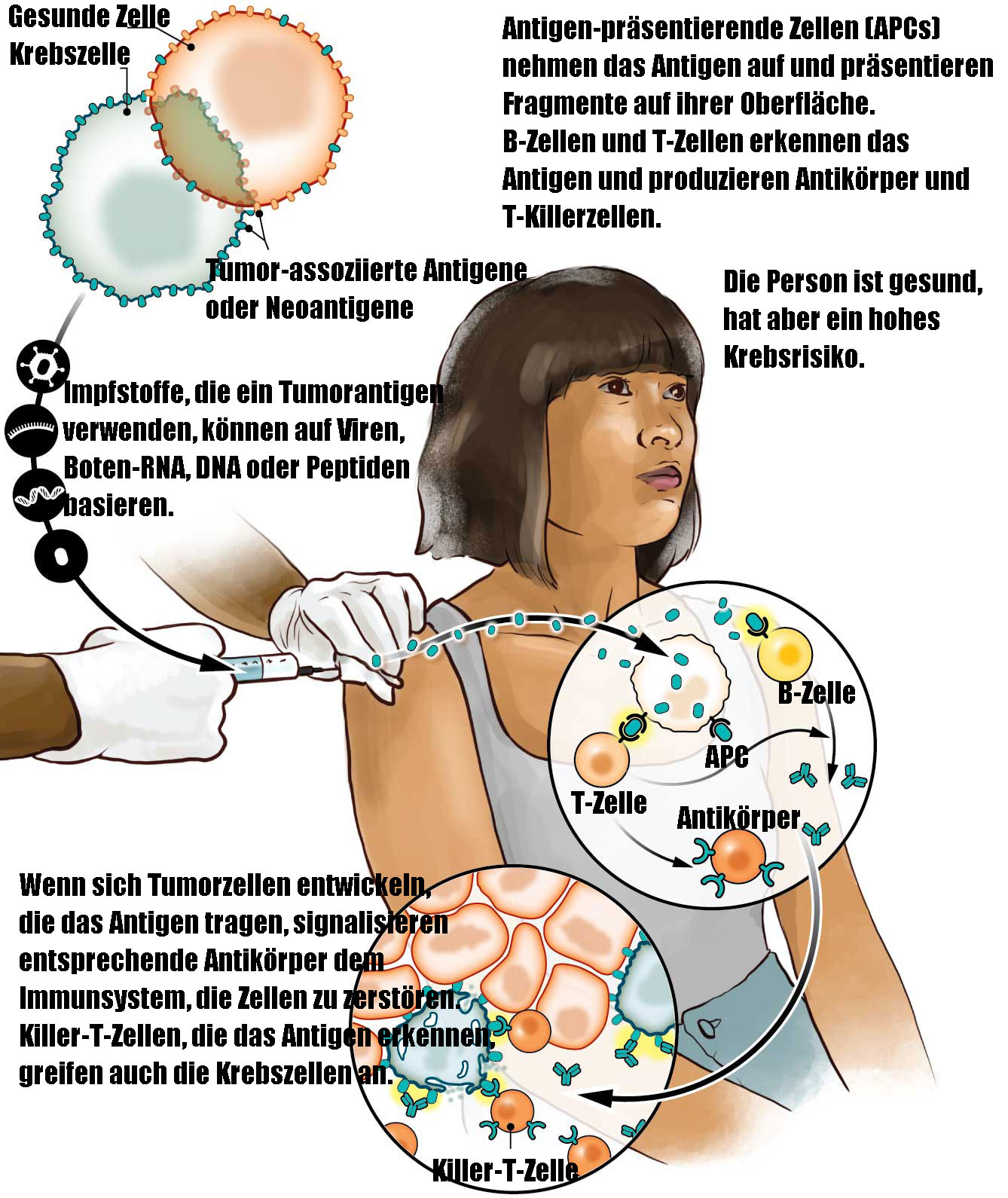
*Abfangen von Krebs – Präventive Krebsimpfstoffe liefern Proteine, die als Tumorantigene bekannt sind, die auf gesunden Zellen selten, auf Tumoren jedoch reichlich vorhanden sind, oder Neoantigene, die es nur in Tumoren gibt. Die Immunzellen nehmen die Antigene auf und produzieren Antikörper und T-Killerzellen, die beginnende Tumorzellen angreifen und so das Krebswachstum verhindern.
Die Forscher erproben mehrere Impfstoffstrategien. Einige verwenden so genannte Tumorantigene, molekulare Marker, die auf gesunden Zellen selten, auf Krebszellen jedoch reichlich vorhanden sind. Der Lynch-Impfstoff zielt stattdessen auf „Neoantigene“ ab, eine wirksame Art von Antigen, die nur auf Tumorzellen vorkommt. Einige setzen nur ein einziges Antigen ein, während andere eine große Anzahl von Antigenen verwenden, um einen umfassenden Schutz gegen Krebs zu erreichen. Der beste Ansatz ist unklar, und die Entwickler stehen auch vor der schwierigen Aufgabe, den Erfolg zu messen, ohne Jahrzehnte zu warten, bis gesunde Menschen Krebs entwickeln.
Die ersten Versuche sind vielversprechend. Wenn die Idee funktioniert, um eine oder einige wenige Krebsarten zu verhindern, könnte sie erweitert werden, um ein ehrgeiziges Ziel zu erreichen, das von Präsident Joe Biden vorgeschlagen wurde: die Entwicklung eines Impfstoffs, der viele Krebsarten verhindern könnte, nach dem Vorbild der Boten-RNA-Impfstoffe (mRNA), die bei der Bekämpfung der COVID-19-Pandemie geholfen haben. „Wir sind weit entfernt von einem allgemeinen Impfstoff“ zur Krebsvorbeugung, sagt die medizinische Onkologin Shizuko Sei von der Abteilung für Krebsprävention des National Cancer Institute. „Aber es könnte in ferner Zukunft sein. Es ist ein schrittweiser Ansatz.“
Die Bemühungen, das Immunsystem zur Krebsbekämpfung zu nutzen, haben eine lange Geschichte. In den 1890er Jahren berichtete der Arzt William Coley, dass die Injektion von Bakterientoxinen – eine Art Impfstoff – die Tumore von Patienten manchmal schrumpfen ließ, offenbar durch Stimulierung des Immunsystems. Jahrzehnte später entdeckten Forscher, dass Immunzellen, so genannte T-Zellen, Tumorantigene als fremd erkennen und Krebserkrankungen angreifen können. Diese Erkenntnis führte zu zwei Klassen zugelassener Therapien: Medikamente, die die molekularen Bremsen der T-Zellen aufheben, so dass sie ihre Krebsbekämpfung intensivieren können, und T-Zellen, die so entwickelt wurden, dass sie sich auf Krebszellen konzentrieren. Beide Arten der Behandlung haben bei bestimmten Krebsarten beachtliche Erfolge erzielt.
Eine dritte Art der Immuntherapie, Impfstoffe zur Behandlung von Krebs, hat sich verzögert. In den frühen 1990er Jahren nahmen die Bemühungen Fahrt auf, als Forscher begannen, Dutzende von Tumorantigenen zu zählen, die die Immunabwehr eines Patienten wecken könnten. Oft handelt es sich bei diesen Antigenen um Proteine, die Krebszellen zum Wachsen oder zur Ausbreitung nutzen, so dass die Antigene gute Marker für Krebszellen sind.
Doch trotz vielversprechender Daten aus Tierversuchen gelang es den meisten Behandlungsimpfstoffen nicht, das Tumorwachstum bei Menschen zu stoppen. Da tumorassoziierte Antigene auch in geringen Mengen auf normalen Zellen vorhanden sein können, tendiert das Immunsystem dazu, sie zu ignorieren. Die Chemotherapie oder andere harte Behandlungen, die Krebspatienten erhalten, schwächen ebenfalls ihre Immunreaktion, und Tumore werden durch ihre „Mikroumgebung“ geschützt – Zellen und Moleküle in der Umgebung, die T-Killerzellen unterdrücken und sie am Eindringen in den Tumor hindern. Der einzige zugelassene Behandlungsimpfstoff für fortgeschrittenen Prostatakrebs verlängert das Leben um nur 4 Monate.
Einige Wissenschaftler waren der Meinung, dass Krebsimpfstoffe besser zur Vorbeugung als zur Behandlung der Krankheit geeignet seien. Eine Befürworterin war die Krebsimmunologin Olivera Finn von der Universität Pittsburgh, deren Team 1989 das erste tumorassoziierte Antigen entdeckte: eine Version von MUC1, einem zuckerhaltigen Zelloberflächenprotein. Die veränderte Version weist auf viele Arten von Krebszellen hin.
Wir sind inspiriert, denn die Auswirkungen werden gewaltig sein.
-Robert Vonderheide/Penn Medicine
Finn entwickelte einen Impfstoff, der aus kurzen Abschnitten von MUC1 besteht. In der ersten Studie über einen präventiven Impfstoff bei gesunden Menschen testete sie die Sicherheit bei 39 Personen, die zuvor präkanzeröse Dickdarmpolypen hatten, die ein erhöhtes Risiko für Dickdarmkrebs darstellen. Im Jahr 2013 berichtete ihr Team, dass 17 von ihnen eine starke Immunreaktion zeigten, mit viel höheren Antikörperspiegeln gegen die Tumorversion von MUC1 als zuvor bei Krebspatienten beobachtet, die den Impfstoff als Behandlung erhielten. Die anderen 22 Personen, die keine Antikörper bildeten, hatten immunsupprimierende Zellen im Blut, die offenbar noch von den entfernten Polypen stammten, so Finn.
Der bescheidene Erfolg der Studie führte zu einer größeren, placebokontrollierten Studie, in der untersucht werden sollte, ob der Impfstoff neue Polypen bei Personen verhindert, denen sie entfernt worden waren. Diesmal produzierten nur 11 von 53 Teilnehmern, die den Impfstoff erhielten, reichlich Antikörper, möglicherweise weil die immunsupprimierenden Polypen der Patienten erst kürzlich entfernt worden waren. Aber unter den 11 Respondern traten nur bei drei von ihnen innerhalb eines Jahres nach der Impfung erneut Polypen auf, verglichen mit 31 von 47 Teilnehmern in der Placebogruppe, berichtet Finns Team in einer in einer Fachzeitschrift veröffentlichten Arbeit.
„Das war sehr ermutigend“, sagt Finn. „Wenn bei Respondern kein Rückfall auftritt, weiß man, dass der Impfstoff wirkt. Die Hinzunahme einer Behandlung, die immunsupprimierende Zellen blockiert, könnte die Ansprechraten erhöhen, sagt sie. Ihr Team plant nun Versuche mit dem MUC1-Impfstoff für verschiedene Krebsvorstufen.
Ein Nachteil von Finns Impfstoffstrategie ist, dass die kurzen Proteine oder Peptide, die er enthält, hauptsächlich einen Teil des Immunsystems anregen: die B-Zellen, die Antikörper bilden. „Für eine Immunität gegen Krebs müssen wir wirklich T-Zellen mobilisieren“, sagt der Krebsimmunologe Robert Vonderheide, Direktor des Abramson Cancer Center von Penn Medicine. Dies geschieht am besten durch Injektion der genetischen Anweisungen für das Antigen und nicht des Antigens selbst. Spezielle Immunzellen nehmen dann die DNA oder RNA auf, stellen das Antigen her, zerkleinern es und bringen die auf das Immunsystem der betreffenden Person zugeschnittenen Teile auf ihrer Zelloberfläche an. Diese Antigen-präsentierenden Zellen bringen dann den T-Zellen bei, Tumorzellen zu erkennen und abzutöten.
Vonderheides Team testet einen DNA-basierten Impfstoff, der auf ein anderes Antigen abzielt, das viele Tumore kennzeichnet: hTERT, ein kleines Stück Telomerase, ein Enzym, das die Chromosomen schützt, wenn sich die Krebszellen vermehren.
Die Ergebnisse einer Studie, in der die Sicherheit des Impfstoffs bei 93 Patienten getestet wurde, die nach einer Behandlung gegen verschiedene Krebsarten in Remission waren, waren ermutigend. Bis auf vier Personen bildeten alle T-Zellen, die sich auf hTERT konzentrieren, berichtete das Team im Juli 2021 im Journal for ImmunoTherapy of Cancer. Und es gab einen Hinweis darauf, dass der Impfstoff den Krebs abwehrte. Von den 34 Personen, die an Bauchspeicheldrüsenkrebs erkrankt waren, waren 41 % nach 18 Monaten noch krebsfrei. Bei anderen Patienten mit Bauchspeicheldrüsenkrebs, die sich in Remission befinden, tritt der Tumor im Durchschnitt innerhalb von 12 Monaten wieder auf.
Das Team in Penn untersucht jetzt die Sicherheit und die Immunreaktionen auf den Impfstoff bei 16 Personen, die nach einer früheren Krebserkrankung in Remission sind und Mutationen in BRCA1 oder BRCA2 geerbt haben, relativ häufige Krebsgene, die das Risiko für Brustkrebs und einige andere Krebsarten erhöhen. Nächstes Jahr wollen die Forscher den Impfstoff an 28 Personen mit BRCA-Mutationen verabreichen, die noch nie an Krebs erkrankt waren.
Impfstoffe zur Krebsprävention auf dem Prüfstand
Zu den geplanten und laufenden klinischen Tests von Impfstoffen zur Krebsprävention gehören die folgenden:
| Ziel-Krebsarten | Teilnehmer | Anzahl der Teilnehmer | Datum des Beginns | Antigene | Art des Impfstoffs |
| Brust, Eierstöcke, Prostata | Menschen mit BRCA1- oder BRCA2-Mutationen, die noch nie an Krebs erkrankt waren oder sich in Remission befinden | 44 | April 2021 | hTERT, PMSA, WNT1 | DNA |
| Dreifach negative Brust | Menschen in Remission nach Behandlung von dreifach negativem Brustkrebs | 24 | Oktober 2021 | Alpha-Laktalbumin | Eiweiß |
| Bauchspeicheldrüse | Menschen mit einer vererbten Mutation oder einer Familiengeschichte, die ein hohes Risiko für Bauchspeicheldrüsenkrebs darstellt | 25 | Mai 2022 | KRAS | Peptid |
| Dickdarm, Endometrium, andere | Menschen mit Lynch-Syndrom, die noch nie an Krebs erkrankt waren oder sich in Remission befinden | 45 | Juni 2022 | Eine Reihe von 209 Frameshift-Neoantigenen | Viraler Vektor |
Da hTERT aber sowohl auf normalen als auch auf Krebszellen vorkommt, könnte ein Impfstoff einen Autoimmunangriff auf gesunde Zellen auslösen, meint der Immunologe Vincent Tuohy von der Cleveland Clinic. Er hat einen Impfstoff zur Vorbeugung von Brustkrebs entwickelt, der möglicherweise sicherer ist, weil er ein Brustzellprotein namens Alpha-Lactalbumin enthält, das nur in der späten Schwangerschaft und während des Stillens gebildet wird. Dieses Protein wird auch bei dreifach negativem Brustkrebs, einer aggressiven Form der Krankheit, produziert. Tuohys Team testet, ob sein Proteinimpfstoff bei 24 Frauen, die wegen dreifach negativem Brustkrebs behandelt wurden und nicht schwanger werden wollen, eine Immunreaktion hervorrufen kann. Der nächste Schritt, so Tuohy, wird eine Studie an gesunden Frauen mit BRCA1-Mutationen sein, die für diese Krebsart anfällig sind.
Andere Teams hoffen, einen breiteren Schutz gegen Brustkrebs zu bieten. Unbeirrt davon, 2012 als „fehlgeleitet“ bezeichnet worden zu sein, steht die NBCC kurz davor, einen Brustkrebsimpfstoff zu testen, zunächst an gesunden Brustkrebsüberlebenden. Die Präsidentin der Gruppe, Fran Visco, sagt, sie habe sich das ehrgeizige Ziel gesetzt, weil sie „frustriert war über den Mangel an Innovation bei Brustkrebs“. Gemeinsam mit Partnern aus der Wissenschaft hat sie sich auf einen Impfstoff geeinigt, der sechs Tumorantigene kombiniert, darunter hTERT und MUC1. „Wir wissen nicht, welche Art von Brustkrebs eine Frau bekommen wird“, erklärt Studienleiter Keith Knutson, ein Immunologe an der Mayo Clinic. Mehrfachimpfstoffe „werden wahrscheinlich wirksamer sein als Impfstoffe, die auf ein einzelnes Protein abzielen“, sagt die Krebsimmunologin Nora Disis von der University of Washington in Seattle, die einen solchen Impfstoff zur Vorbeugung von Darmkrebs entwickelt.
Während einige Teams versuchen, die durch Krebsimpfstoffe ausgelöste Immunreaktion zu erweitern, wollen andere sie sicherer und präziser machen, indem sie auf Neoantigene abzielen, die nur auf Krebszellen vorkommen. Diese Bemühungen haben sich in den letzten zehn Jahren dank der zunehmenden Sequenzierung von Tumorgenomen, die eine Flut von Neoantigenen zutage gefördert hat, beschleunigt. Einige treiben das Krebswachstum an, während andere keine offensichtliche Funktion haben. Die meisten sind einzigartig für einen einzelnen Krebs – ein Hindernis für die Entwicklung präventiver Impfstoffe, die auf Marker abzielen müssen, die im Voraus vorhergesagt werden können.
Einige Neoantigene treten jedoch bei vielen Menschen zuverlässig in ihren Tumoren auf. Bauchspeicheldrüsenkrebs zum Beispiel wird fast immer durch Mutationen in einem Wachstumsprotein namens KRAS ausgelöst, die eine vorhersehbare Reihe von Neoantigenen hervorrufen. In diesem Frühjahr werden die Immunologin Elizabeth Jaffee und ihre Kollegin Neeha Zaidi von der Johns Hopkins University damit beginnen, einen Impfstoff, der mutierte KRAS-Peptide enthält, an 25 Männern und Frauen zu testen, die noch nicht an Krebs erkrankt sind, aber aufgrund einer vererbten Mutation oder einer familiären Vorgeschichte ein hohes Risiko aufweisen. KRAS ist so etwas wie die Achillesferse von Bauchspeicheldrüsenkrebs, sagt Jaffee: Es ist das erste von mehreren Genen, das mutiert wird. Daher hofft das Team, dass frühe Tumorzellen nicht in der Lage sein werden, den Impfstoff zu umgehen, indem sie KRAS ausschalten und einen anderen Weg zum Wachstum finden.
Krebserkrankungen des Lynch-Syndroms weisen auch eine vorhersehbare Anzahl von Neoantigenen auf. Das liegt daran, dass das DNA-Reparaturproblem der Patienten zu „Frameshift“-Mutationen führt, die die Art und Weise verändern, wie die Proteinbildungsmaschinerie einer Zelle ein Gen abliest, und das daraus resultierende Protein in einer konsistenten Weise verschlüsseln. Ein Peptidimpfstoff, der einige dieser Neoantigene enthält und von einem deutschen Team entwickelt wurde, verursachte bei Tests an Krebspatienten keine ernsthaften Nebenwirkungen. Ein ähnlicher Impfstoff, der für Mäuse mit Lynch-Syndrom entwickelt wurde, verringerte das Tumorwachstum, berichteten die Forscher im Juli 2021 in der Zeitschrift Gastroenterology.
Der Impfstoff, den das Team um Vilar-Sanchez testen wird, ist ehrgeiziger: Er besteht aus Viren, die so modifiziert sind, dass sie die DNA für sage und schreibe 209 Frameshift-Neoantigene tragen, die in Lynch-Tumoren vorkommen. Die Immunsysteme der Menschen reagieren unterschiedlich auf bestimmte Neoantigene, und die Tumore verschiedener Personen bilden nicht alle die gleiche Menge. „Daher ist es am besten, wenn man viele davon hat“, sagt Elisa Scarselli, Chief Scientific Officer von Nouscom, einem italienischen Unternehmen, das den Impfstoff entwickelt.
Der Impfstoff wird auch als Behandlung entwickelt. In einem frühen Test verabreicht Nouscom ihn zusammen mit einem Immuntherapie-Medikament an Patienten mit metastasierendem Krebs mit Frameshift-Mutationen, wie sie beim Lynch-Syndrom auftreten. Auf einer Tagung im Herbst 2021 berichtete das Unternehmen, dass die Behandlung bei sieben der ersten 12 Patienten die Tumore schrumpfen ließ. „Wir glauben wirklich, dass wir bei gesunden Trägern der Lynch-Krankheit eine noch stärkere Immunogenität feststellen werden“, weil sie ein stärkeres Immunsystem haben sollten, so Scarselli.

In der Studie von Vilar-Sanchez, die in wenigen Monaten beginnt, wird der Impfstoff 45 Freiwilligen mit Lynch-Syndrom verabreicht – sowohl Menschen, die sich nach einer Krebsbehandlung in Remission befinden, als auch anderen, die nie einen Tumor hatten. Die Forscher werden prüfen, ob der Impfstoff eine Immunreaktion auslöst und sich auf Polypen oder Tumorbildung auswirkt.
Wenn die Ergebnisse gut aussehen, wird der nächste Schritt eine randomisierte Studie mit Hunderten von Patienten über vielleicht 5 bis 10 Jahre sein. „Es gibt viel zu gewinnen“, wenn der Impfstoff funktioniert, sagt Vilar-Sanchez. „Ein Krebsimpfstoff wird das Risiko nicht auf Null reduzieren, aber er könnte einen Einfluss darauf haben, wie oft wir Vorsorgeuntersuchungen durchführen. Der Impfstoff könnte Patienten auch bei der Entscheidung helfen, ob sie sich einer Hysterektomie unterziehen sollten, um Gebärmutterkrebs zu verhindern, der bei Menschen mit Lynch-Syndrom häufig auftritt.
Für alle Präventionsimpfstoffe wäre es ein langer Weg bis zur Zulassung, wenn die Forscher auf das Auftreten von Tumoren warten müssten, um die Wirksamkeit des Impfstoffs zu beurteilen. Daher werden sie auch nach Ersatzmaßstäben für den Schutz suchen, z. B. nach einem geringeren Wachstum von Polypen bei Menschen, die zu Darmkrebs neigen. Für Brustkrebs haben die Forscher noch keine Biomarker, hoffen aber, sie zu finden, vielleicht eine Veränderung in Immunzellen im Blut oder im Brustgewebe, sagt Vonderheide.
„Wir müssen klug genug sein, um der FDA [U.S. Food and Drug Administration] einen Biomarker für den Erfolg zu präsentieren“, sagt Vonderheide. „Das ist eine gewaltige Aufgabe. Aber wir sind inspiriert, denn die Auswirkungen werden enorm sein.“
Unabhängig davon, welche Antigene sie bevorzugen, gehen viele Wissenschaftler davon aus, dass sie ihre nächsten präventiven Impfstoffe nach dem Vorbild der führenden COVID-19-Impfstoffe entwickeln werden, bei denen ein Lipidpartikel verwendet wird, um mRNA für Antigene in die Zellen zu transportieren. mRNA-Impfstoffe sind einfacher herzustellen und zu verabreichen als DNA- oder Virusimpfstoffe, und die Pandemie hat gezeigt, dass sie im Allgemeinen sicher sind und eine starke Reaktion hervorrufen. „Die Tatsache, dass sich mRNA-Impfstoffe bei Milliarden gesunder Menschen jeden Alters als sicher erwiesen haben, macht [mRNA] zu einer sehr guten Plattform“ für präventive Krebsimpfstoffe, so Jaffee.
Auch das Weiße Haus hat es auf mRNA-Impfstoffe zur Krebsprävention abgesehen. Sie stehen auf der Liste potenzieller Projekte für den wiederbelebten „Cancer Moonshot“ und die neue Forschungsagentur „Advanced Research Projects Agency for Health“ (ARPA-H), die mit hohem Risiko und hohen Gewinnen verbunden ist. In einem Konzeptpapier für ARPA-H wird das Ziel folgendermaßen formuliert: „Verwenden Sie mRNA-Impfstoffe, um dem Immunsystem beizubringen, 50 häufige genetische Mutationen zu erkennen, die Krebs auslösen, so dass der Körper Krebszellen auslöscht, wenn sie zum ersten Mal auftreten.“
Diese Beschreibung lässt einige Augenbrauen hochziehen. „Das wäre heldenhaft“, sagt Finn, denn die Impfstoffantigene müssten nicht nur eine riesige Anzahl von Krebsmutationen abdecken, sondern auch „die unglaubliche genetische Vielfalt“ der individuellen Immunreaktionen. „Das ist nicht unmöglich, aber auch nicht einfach“, sagt sie.
Der klinische Genetiker Steven Lipkin von Weill Cornell Medicine, der an Impfstoffen für das Lynch-Syndrom arbeitet, ist vorsichtig optimistisch und stellt fest, dass ein Impfstoff, der die Raten der häufigsten Krebsarten „bei einer großen Anzahl von Menschen um ein Drittel oder die Hälfte senken würde, ein enormer Vorteil wäre“.
Ein Team testet bereits einen Impfstoff zur Vorbeugung von Multikrebs – zwar noch nicht an Menschen, aber an Hunden. In einer fünfjährigen Studie verabreicht ein Team 400 Hunden mittleren Alters einen Impfstoff, der 31 Antigene von acht häufigen Hundekrebsarten enthält. (Weitere 400 Hunde erhalten einen Placebo-Impfstoff.) Der Impfstoff stützt sich auf RNA-Neoantigene, wenig untersuchte Moleküle, die durch RNA-Verarbeitungsfehler und nicht durch Mutationen in der DNA entstehen. Sie kommen bei Hunden und Menschen viel häufiger vor als DNA-Neoantigene und sind „hoch immunogen“, sagt der Entwickler und Biochemiker Stephen Johnston vom Biodesign Institute der Arizona State University in Tempe. Wenn sie sich als wirksam erweisen, könnten sie es leichter machen, das Ziel des Weißen Hauses zu erreichen, einen Impfstoff gegen Krebs beim Menschen zu entwickeln, sagt er.
Ein weiterer Befürworter eines universellen Impfstoffs zur Krebsprävention ist der Krebsgenetiker Bert Vogelstein von der Johns Hopkins University. Er stellt fest, dass die Sequenzierung gezeigt hat, dass „eine relativ kleine Anzahl von Genen an den meisten Krebsarten beteiligt ist“, was darauf schließen lässt, dass eine begrenzte Anzahl von Antigenen zu einem breiten Schutz führen könnte. Ein solcher Impfstoff „scheint wie Science Fiction“, sagt Vogelstein, aber „eine konzertierte Anstrengung vieler Labors“ könnte Erfolg haben. Sei stimmt ihm zu: „Das ist nicht verrückt. Das ist möglich.“
Für Dave Dubin könnte sogar ein kleinerer Erfolg – ein Impfstoff gegen das Lynch-Syndrom – „eine große Veränderung bedeuten“, sagt er, wenn er weniger Krebsvorsorgeuntersuchungen und keine größeren Operationen mehr bedeutet. „Das Ziel wäre, ein fast normales Leben zu führen.